O que você acha que é comum entre gotículas de água aderentes ao vidro, insetos andando na água e pingentes de gelo pendurados no inverno nos beirais da sua casa? Como as pessoas na multidão, as moléculas do líquido e, portanto, a água, se apegam uma à outra, abrindo caminho.
Por que a água forma gotas?

É essa propriedade que permite que o líquido preencha todos os cantos e lacunas do tanque onde é derramado. Embora as moléculas de líquidos se movam em relação umas às outras mais livremente que as moléculas de sólidos, elas ainda não são absolutamente livres, mas atraídas uma pela outra. As moléculas de água não estão tão intimamente ligadas, como, por exemplo, as moléculas de mel. Portanto, o mel não é tão fluido quanto a água, mas é um líquido denso, grosso e xaroposo. Se sabão é adicionado à água, a tensão superficial da água diminui.
Atração mútua e superfície
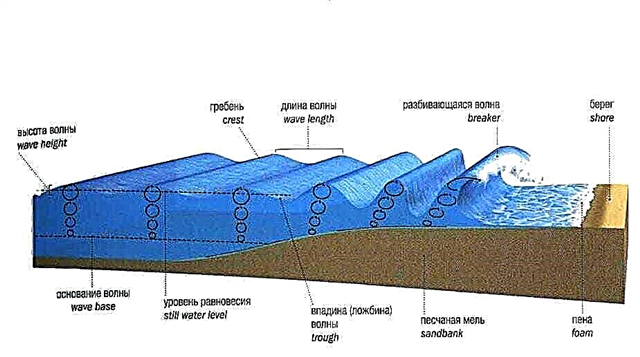
Como as moléculas líquidas experimentam atração mútua, líquidos, como sólidos, formam superfícies. Em contraste, as moléculas de gás, sem experimentar atração mútua, se espalham em todas as direções. A força da atração que mantém as moléculas de água juntas em sua superfície é chamada tensão superficial. A tensão superficial é a força que permite que alguns insetos andem na água como no chão sem molhar as patas.
Seus corpos são muito leves e a tensão superficial mantém esses insetos na superfície, impedindo-os de mergulhar na água.A tensão superficial dá a pequenas porções de água a forma de gotas redondas. As moléculas de água são atraídas uma pela outra, mas não experimentam atração pelas moléculas do ar circundante. Portanto, pequenos "pedaços" de água formam gotículas de formato esférico.
Por que as gotas se formam no vidro?
Quando você bebe, um copo de água, as gotas restantes grudam nas paredes do copo e não vazam, mesmo que o copo fique de cabeça para baixo por um longo tempo, porque as moléculas de água não são atraídas pelas moléculas de ar, mas são muito bem atraídas pelas moléculas de vidro. No final, grandes quedas sob a influência da gravidade caem. Mas gotas pequenas e leves permanecem teimosamente no lugar. As moléculas de vidro contêm moléculas de água em seus fortes braços elétricos.

De fato, sua atração mútua é tão grande que a água em um copo molhado é frequentemente distribuída em uma fina camada na superfície do copo sem formar gotas. Se você tentar sacudir a água, ela escorrerá até a borda do copo e permanecerá ali, incapaz de se separar do seu amado copo. A água não consegue aderir apenas a certas superfícies. Por exemplo, se você polvilhar um pouco de água sobre papel de cera, a água se acumulará em gotas e deslizará sem deixar rastro da superfície encerada.
Fato interessante: a tensão superficial permite que alguns insetos andem na água.
Só há uma maneira de derramar toda a água de um copo sem deixar vestígios: adicione um pouco de sabão à água. Sabões e outros detergentes - detergentes - reduzem a tensão superficial da água.Ao lavar os detergentes para a roupa, evite que a água molhe a superfície do tecido, de modo que o tecido seja ensopado com uma solução de lavagem. Juntamente com a água, um detergente penetra no tecido. Se você lavar o copo com água e sabão, algumas gotas grudam nas paredes. A maior parte da água, juntamente com o sabão, será derramada de um copo.